如果有这样一台“加速器”,您想快进到哪一步?
Q1:您知道如何更加高效快速做好肽图实验吗?
A:UHPLC配合小粒径核-壳技术色谱柱可对抗体酶解后的大量色谱峰实现良好的分离。优异的保留时间重复性完全满足样品特性和变异检测时进行洗脱峰的比较需求
HPLC肽图分析是蛋白质一级结构研究中极为重要的手段之一,不但可以比较重组与天然蛋白质结果之间的同一性,确认基因工程上游和下游处理过程中是否发生差错、重组产物中是否存在翻译后修饰及未预期氨基酸的变异等,而且不同批次产品的肽谱比较可验证工艺过程的稳定性。因此,肽图分析在生物技术药物质控中尤为重要。
目前肽图分析常用方法主要是胰蛋白酶切RP-HPLC方法。蛋白样品经酶解后进入HPLC,进行色谱分离,保留时间不同的肽段依次进入紫外检测器进行检测。
岛津的相关液相产品,例如Nexera-i系列、LC-40以及生物惰性兼容液相Nexera Bio均可实现蛋白类药物的HPLC肽图分析。
蛋白类药物肽图分析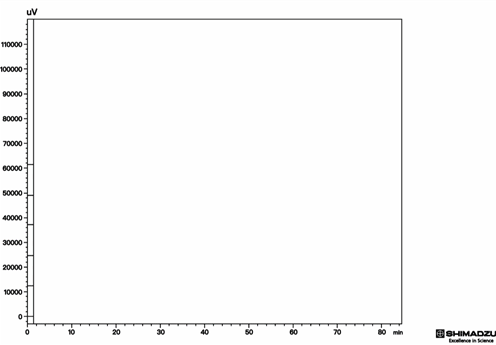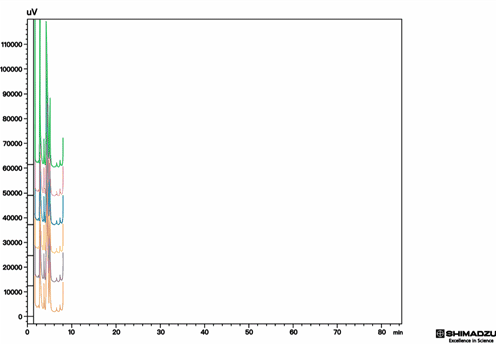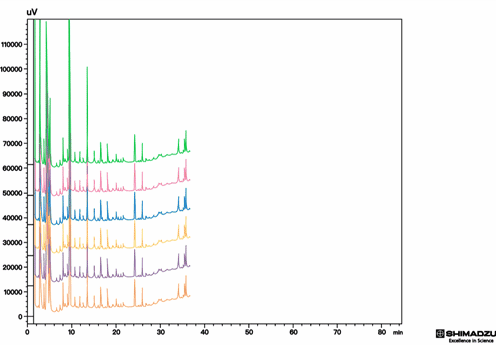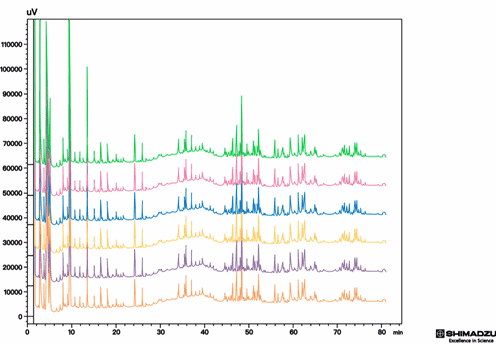
Q2:您想知道如何利用岛津液相产品获取更优秀的抗体电荷变异体分析结果吗?
A:岛津生物惰性兼容液相Nexera Bio系统,更耐腐蚀,而且能减少生物大分子的吸附保证生物大分子的完整性,有效保障分析重复性。
电荷异构体的存在将会影响到蛋白质药物的活性、结合能力、药代动力学、免疫原性及结构稳定性,从而影响药物有效性、安全性及保质期。同时,电荷异质性的控制程度也反映了重组蛋白类药物生产工艺的一致性。因此,在生物类似药的研发及与原研药的一致性评价研究中,电荷异质性是工艺质量控制的重要因素。
为了最大限度地降低蛋白质与固定相填料的离子相互作用及二者之间可能存在的吸附作用,电荷异质性分析通常使用高离子强度的流动相,并且采用碱性或酸性分析条件。但是,高离子强度流动相和碱性/酸性分析条件给液相色谱仪的耐腐蚀性和系统稳定性带来严峻的挑战。
ATP分析

对ATP进行分析并比较峰强度(面积),Nexera Bio表现出5倍的信号强度优势
蛋白类生物药电荷异质体分析
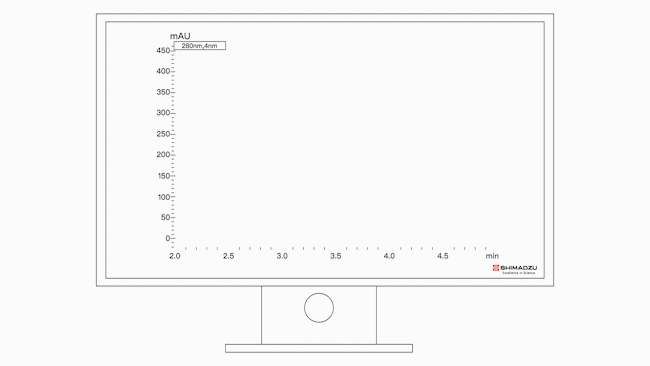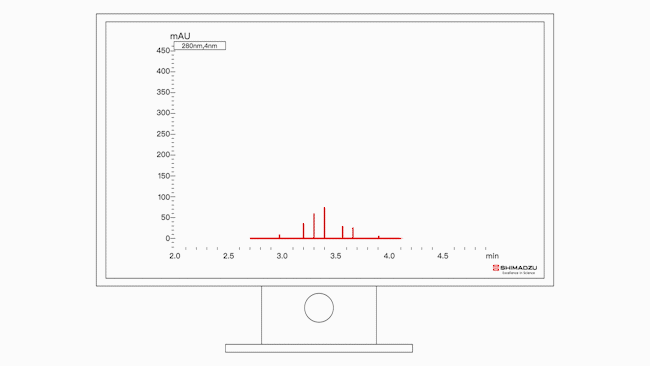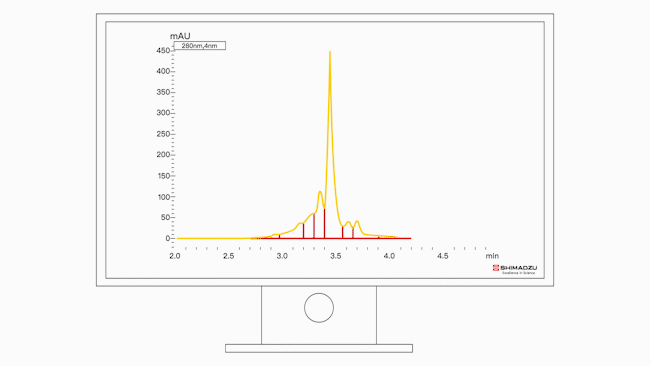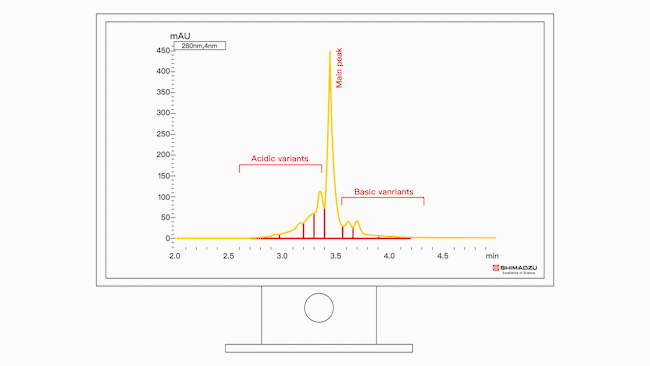
图1:盐梯度方法中贝伐单抗生物仿制药的电荷异质体分布
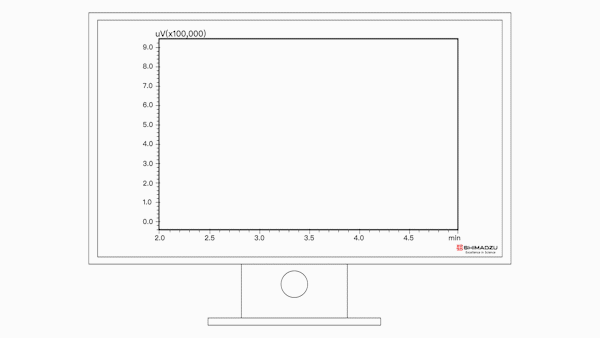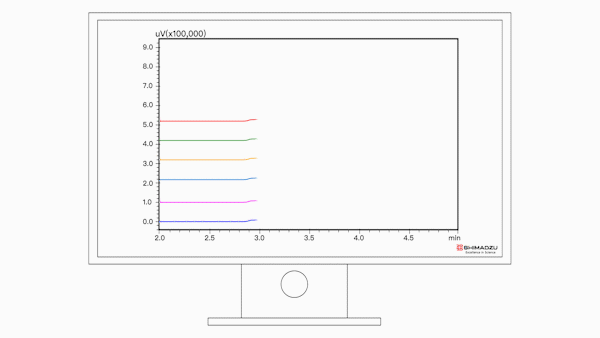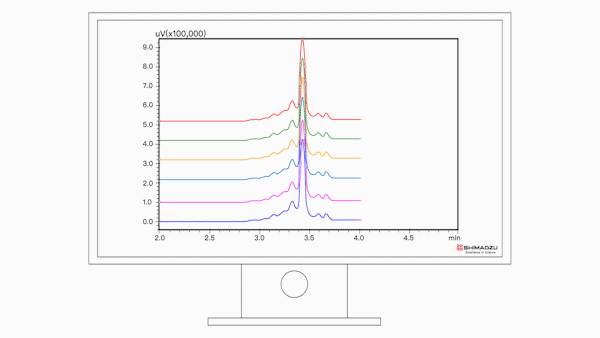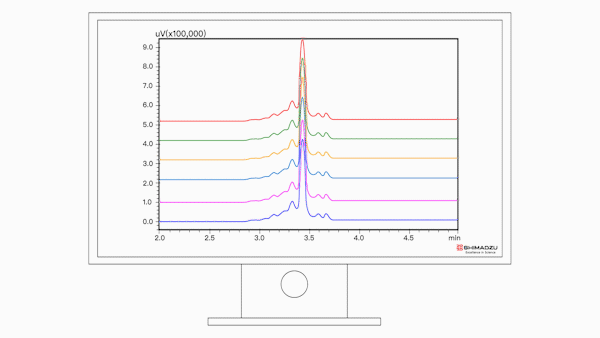
图2:盐梯度方法中贝伐单抗生物仿制药的6次分析UHPLC-UV(280nm)色谱图
Q3:如何轻松掌握抗体唾液酸定量分析的细节?
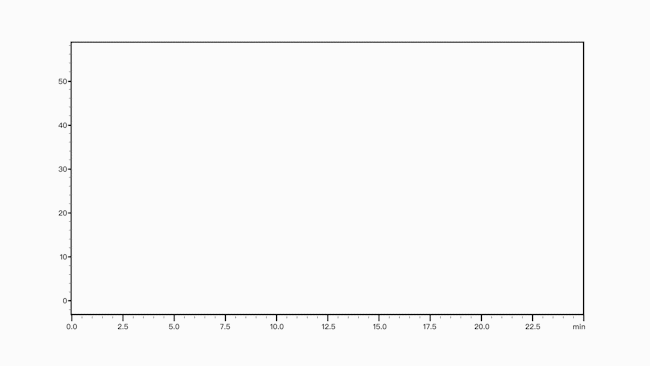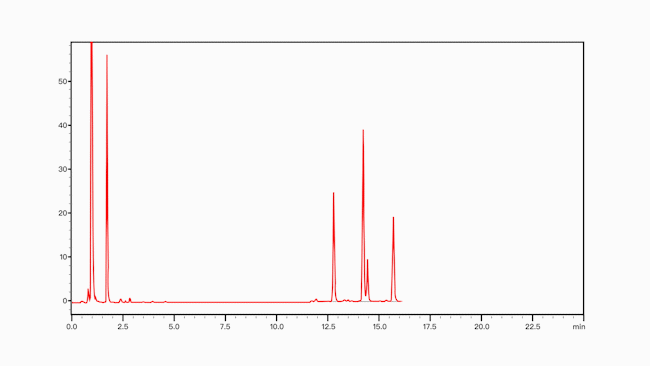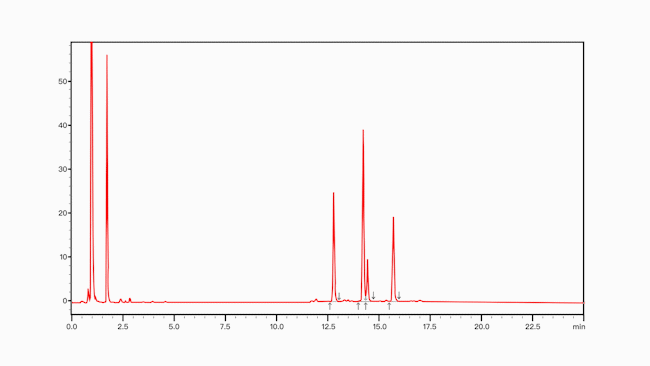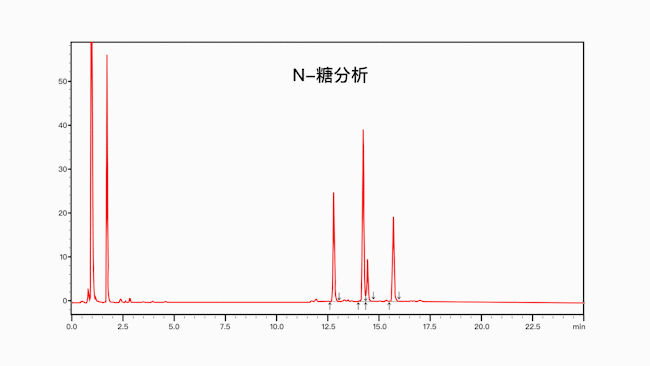
A3:岛津开发了UHPLC测定抗体中唾液酸的分析方法,该方法分析快、重复性好、灵敏度高,适合用于抗体类药物中唾液酸含量的分析。
糖基化是蛋白质的一种重要翻译后修饰,糖基分析主要包含唾液酸含量测定、单糖组成分析、糖基化位点测定、糖链结构测定等。
唾液酸含量的测定是先将唾液酸从糖链上解离成游离状态,再进行化学反应实现衍生化,通过测定衍生化产物从而测定唾液酸含量,常用的方法有间苯二酚显色法和HPLC法。间苯二酚显色法是利用间苯二酚将游离的唾液酸进行衍生生成有色化合物,再用紫外分光光度法测定其含量;HPLC法是利用邻苯二胺(OPD)对唾液酸进行衍生,然后用带紫外检测器的HPLC或者LC-MS/MS进行定量。
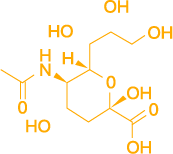
Neu5Ac结构图
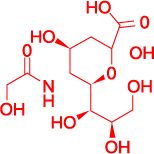
Neu5Gc结构图
蛋白类生物药糖型分析

Q4:利用岛津液相对蛋白纯度分析的关键参数
A4:岛津利用Nexera Bio 生物兼容液相色谱系统和Shim-pack Bio生物惰性尺寸排阻色谱柱,实现了注射用重组人白介素-11、FC融合蛋白、贝伐单抗体生物类似药和阿达木单抗中聚集体的分析。在保证生物大分子的完整性、有效保障分析重复性的同时,为蛋白类药物低聚体分析提供快速、高效的SEC方法。
蛋白质药物在其生产、贮藏、运输、销售以及用药过程中由于外力因素的作用可能会产生聚集。蛋白质聚集现象会导致蛋白药活性和其在药品中的浓度降低,并可能产生有害的毒理学作用和免疫应答,甚至发生危及生命的药物反应。FDA关于聚集体的指导原则中就指出蛋白聚集体在人体内极易产生免疫原性。
对于常见的蛋白质低聚体(二聚~四聚体),非还原型聚丙烯酰胺凝胶电泳( SDS-PAGE )需要在变性条件下进行,一般会影响多聚体的检测。而体积排阻色谱法(SEC)条件温和,不会对蛋白的形态产生较大的影响。因此,SEC法能较准确地检测蛋白质中的低聚体,是蛋白质药物开发、质量控制和稳定性研究中常用的聚集体分析方法。
大小变异体,聚体分析
应用案例:单抗药物聚集体分析,推荐生物惰性液相

Q5:利用岛津液相从容应对氨基酸组成分析
A5:岛津利用性能优异的液相色谱自动进样器,可完成进样器内氨基酸自动柱前衍生并在线进行HPLC分析,从而实现氨基酸样品的自动、高效分析。
作为细胞生长的环境和营养来源,培养基的性能很大程度上决定了细胞密度和表达产物的产量和质量,因此培养基是工艺开发最重要的环节之一。其中,在生产工艺优化和确认过程中,以及QC过程中,细胞上清液中氨基酸含量的监测对细胞培养有着重大的意义。但是,离线衍生后使用HPLC分析,以及HPLC柱后衍生法检测氨基酸等方法,不仅耗时耗力,并且对结果准确度影响较大。因此,开发操作简单、高效稳定的分析方法,对氨基酸组成分析非常有意义。
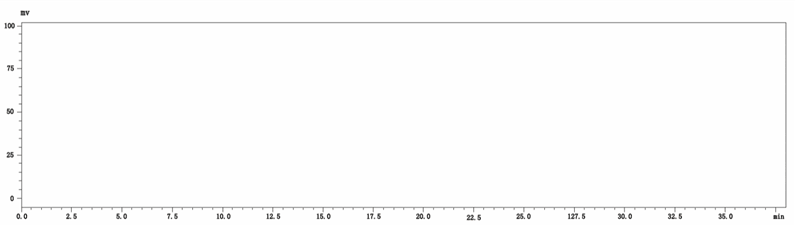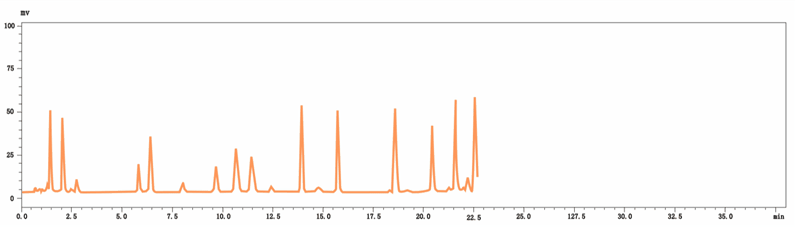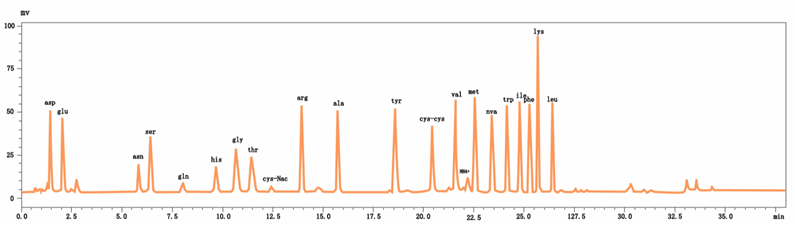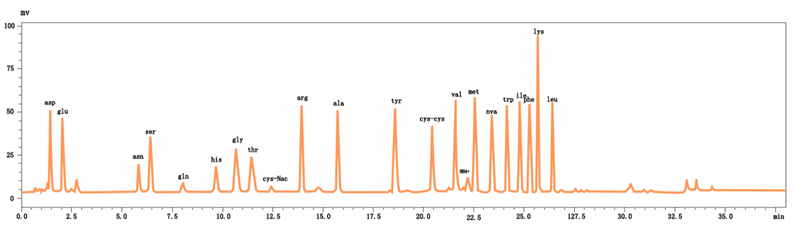
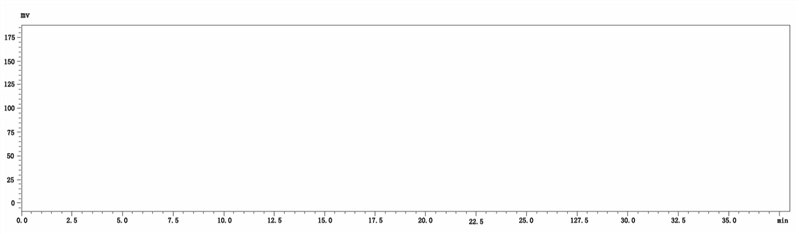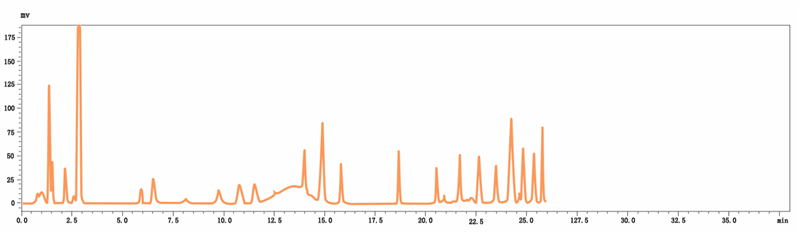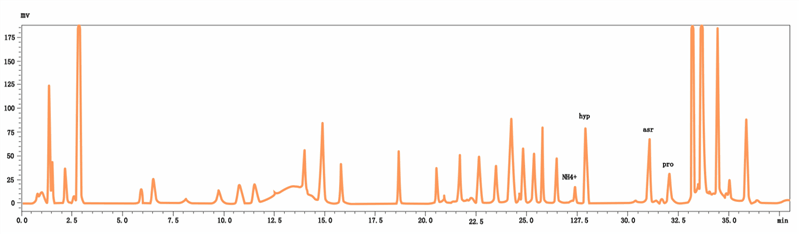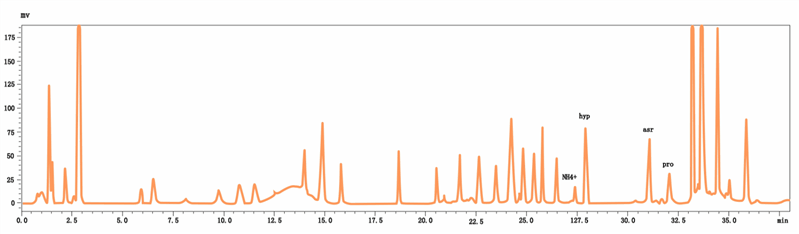
24种氨基酸标准溶液色谱图(双波长同时检测)