药品残留溶剂GCMS检测整体解决方案
残留溶剂分析是药品质量控制的重要组成部分,是相关企业及药品检验实验室的常规检测项目。关于化药中的溶剂残留世界主要国家及组织都有相关规定及标准,如美国药典(USP)通则<467>,欧洲药典(EP)2.4.24,我国药典(ChP2020)四部0861,以及ICH Q3C等,并都根据残留溶剂对人体健康危害性的大小分为1类、2类和3类溶剂。
残留溶剂的检测通常使用顶空气相色谱法(HS-GC-FID)或是顶空气相色谱质谱法(HS-GC/MS),然而GC-FID定性需要使用标准参比溶剂,当峰重叠时很难进行准确的定性。而GC/MS可以根据质谱图信息对难以区分的目标峰和未知峰进行再一次的识别,在药品质量控制及污染原因调查等方面具有明显的优势。另一方面国家药监局对于《药品记录与数据管理要求》的有关规定,加强药品研制、生产、经营、使用活动的记录和数据管理,确保有关信息真实、准确、完整和可追溯,因此对分析仪器的数据完整性也有了更高的要求。
岛津GCMS系统搭配高性能HS-20 NX 顶空进样器和LabSolutions GCMS数据库版工作站,从卓越的硬件性能到合规的数据软件为您提供完整解决方案,全方位把控药品残留溶剂分析。
典型HS-GC-FID/MS分析水溶性药品中|类和2类残留溶剂
按照USP467操作步骤A制备1类、2A类、2B类标准溶液和测试液等水溶性样品溶液,其中2A类标液中添加叔丁醇(t-BuOH和环基甲基迷(CPME)(t-BuOH 和CPME是ICH Q3C(R8)中的两类溶剂)。并按照步骤A的分析条件分别进行HS-GC-FID和HS-GC/MS测试,两种检测器使用相同的色谱柱。
仪器配置:HS-20 NX+GCMS-OP2020 NX+LabSolutions GCMS
恒线速度模式保证高分离效果的同时完美匹配GC-FID和GC/MS方法保留时间,GC分析条件转移无压力。
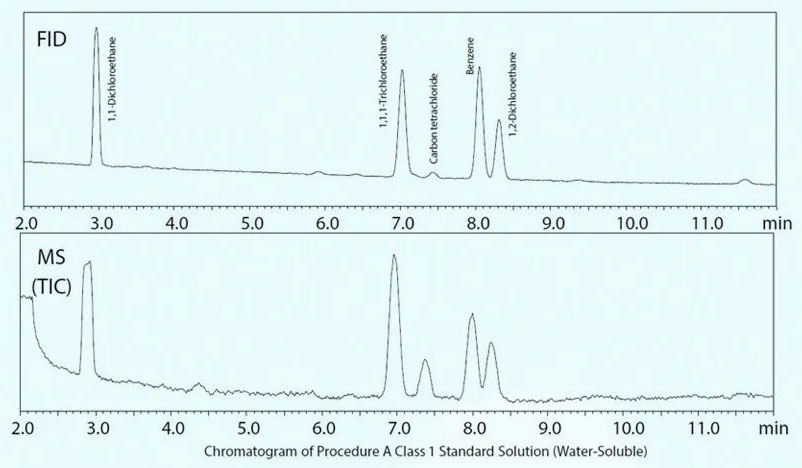
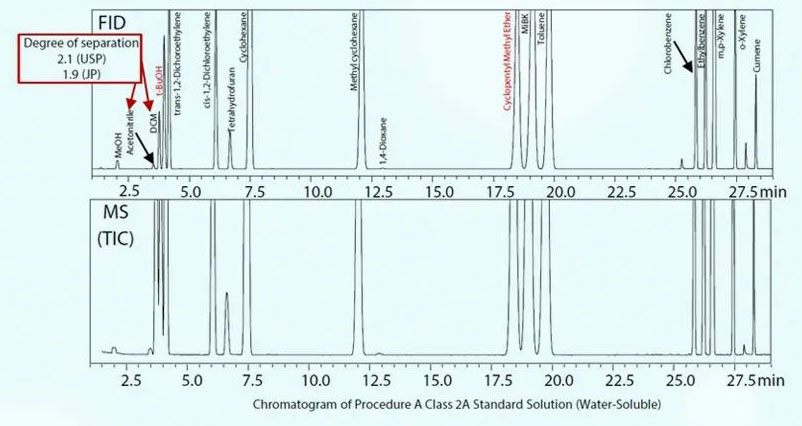
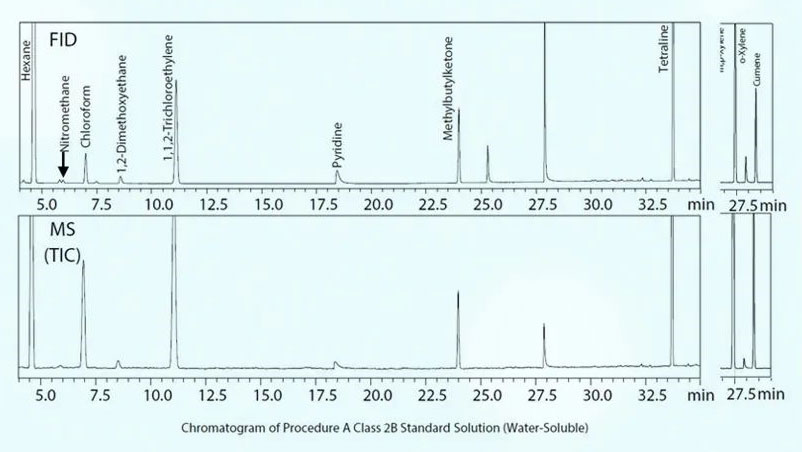
在两种不同检测器中使用相同的色谱柱并以恒定的线速度模式进行分析,可以使所有分析物的峰保留时间相匹配,进而很好的验证FID检测到的峰的质谱图,定性更准确。同时由上述图2可知,添加到2A类标准溶液中的高关注度目标物t-BuOH和CPME(红色标记的化合物)与其他分析物达到很好的分离,恒线速度模式完美应对USP467及药典等标准方法。
GC/MS方法准确定性,防止错误判别
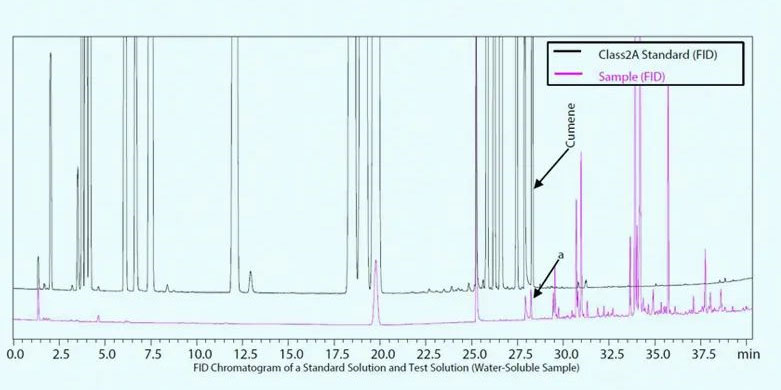
上图2A类标准溶液和水溶性样品溶液的FID色谱图显示,虽然峰a在FID上的保留时间与异丙烯(Cumene)几乎相同,但通过质谱图对比发现其为a-蒎烯,因此使用GC/MS质谱图信息可以很好的防止类似的错误判别,达到准确定性。
LabSolutions GCMS数据库版工作站为安全管理数据保驾护航
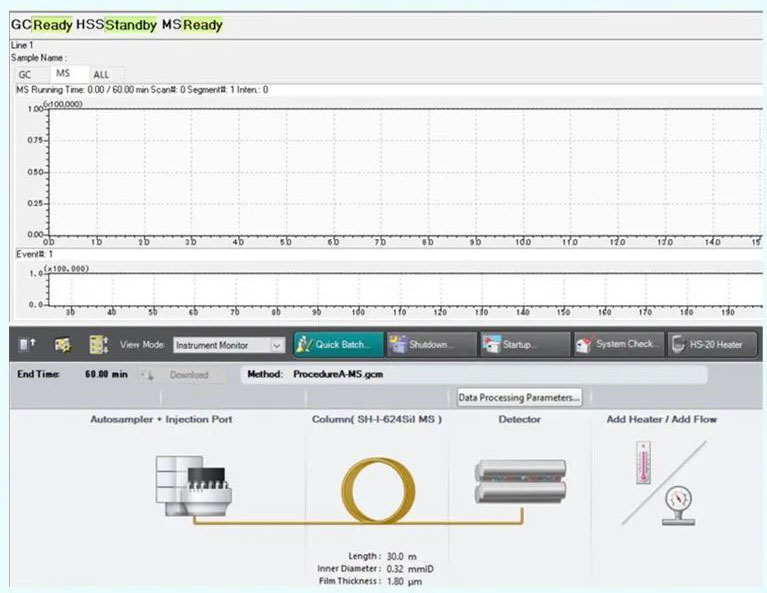
采用LabSolutions集成分析软件进行控制,图形化界面清晰直观,用户友好,该软件可用于GC-FID分析和GC/MS分析,并提供单机版(LabSolutions DB GCMS)和网络版 (LabSolutions CS GCMS),二者均通过数据库进行人员控制和数据管理,简化操作的同时进一步满足数据完整性等合规性要求,保障数据安全。
药品残留溶剂GCMS检测整体解决方案

气相色谱质谱联用仪
-集成高灵敏度和低实验成本
-智能时间管理,高效运行减少停机时间
-LabSolutions Insight让多数据分析更高效
-全惰性化GC/MS流路

顶空进样器
-高温、超短惰性流路,实现高沸点物质的高灵敏度分析;
-加热炉底部进入,大大提高重现性;
-样品加压流路和样品环填充流路分开技术,大幅降低交叉污染;




