解决方案-安全性指标<元素杂质>
在总体修订概述中,重点解析了四部凡例和通则0251药用辅料关于残留溶剂和元素杂质的修订情况。通则0251明确提出,药用辅料残留溶剂和元素杂质的控制应参照相关通则(通则0861和通则0862)和ICH的要求,根据药用辅料的生产工艺和拟应用的制剂需要进行风险评估和相应控制,以确保药用辅料的质量、安全及功能满足制剂的需要。基于风险评估确定需要在标准中列入检查项的,应采用适宜的经过验证的分析方法检测。药用辅料元素杂质风险评估信息表可用于元素杂质风险评估与控制的确认。药品已经按照相关要求进行了元素杂质评估和控制的,其药用辅料可不需要再按《中国药典》药用辅料品种正文中的元素杂质相关检查项目(包括重金属、砷盐及其他ICH Q3D表5.1中的元素的相应检查项目)进行检测来证明符合规定。
据最新文献【1】报道,目前中国药典对含有特定元素杂质检查项的品种开展了评估:
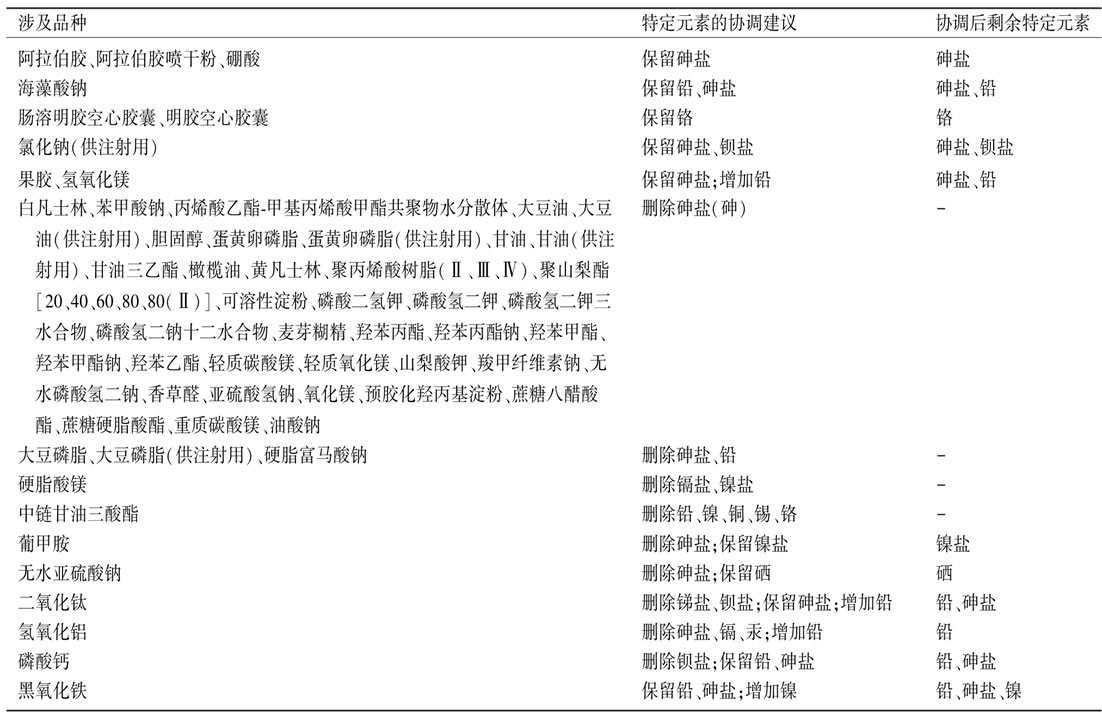
可根据风险评估的原则,对于中等程度风险的元素杂质,在标准中以“注”的形式给出元素杂质的风险提示信息,如下表。
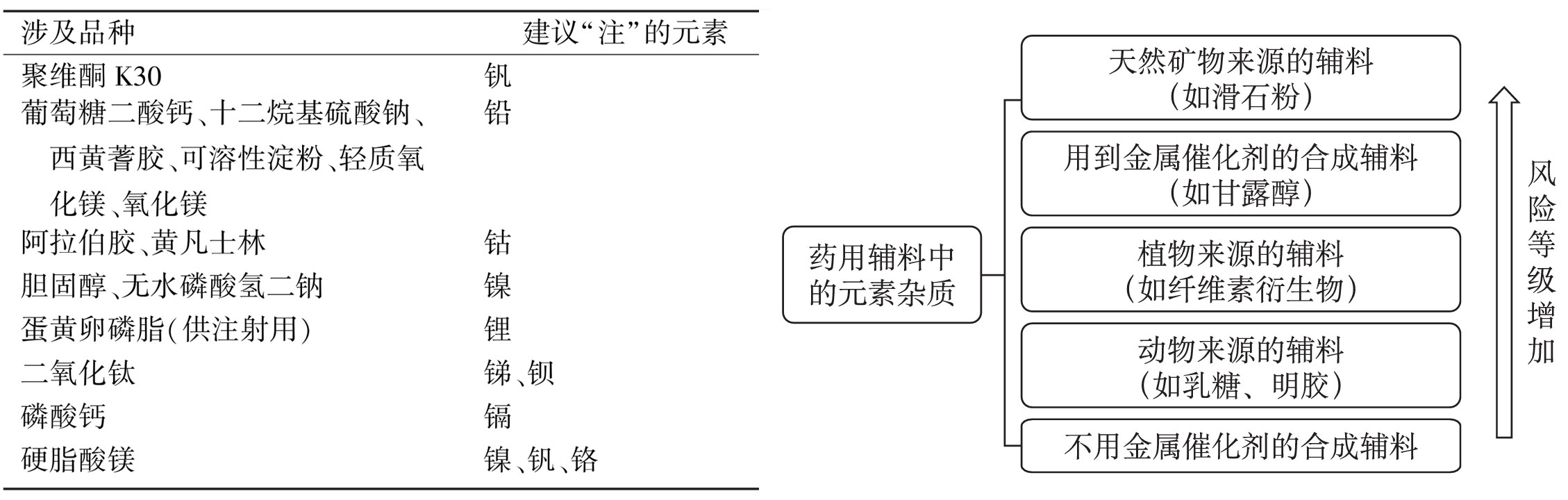
从重金属到元素杂质的转变是方法上、思想上的一次重大转变,涉及企业、监管等各方面的变化,是药品生命周期管理的重要环节。
药用辅料作为药品的一部分,在《中国药典》药用辅料中引入Q3D的控制理念,必然对整个《中国药典》以及药用辅料质量控制起到重要的推进作用。
● 岛津解决方案及典型案例
| 元素杂质分析/鉴定 |
◆ 原子吸收分光光度计(AA-7800) ◆ 电感耦合等离子体发射光谱仪(ICPE-9000) ◆ 电感耦合等离子体质谱仪(ICPMS-2040/2050LF) ◆ 能量色散型X射线荧光光谱仪(ALTRACE、EDX-7200、EDX-8100) |
● 典型案例1-【药用辅料(供注射用)的元素杂质测定】
岛津公司开发了ICPMS法测定难溶性药物包合物注射剂中药用辅料磺丁基倍他环糊精钠元素杂质检测方案。
磺丁基倍他环糊精钠是高水溶性环糊精衍生物能很好地与药物分子包合形成非共价复合物,从而提高药物的稳定性、水溶性、安全性,降低肾毒性、缓和药物溶血性,控制药物释放速率,掩盖不良气味等。磺丁基倍他环糊精钠对含氮类药物具有特殊的亲和力与包合性,已广泛应用于注射药、口服药、鼻部用药、眼部用药。
根据该注射剂在临床中的最大日使用剂量以及参考ICH Q3D的限量要求、USP <233>中 ICP-MS方法程序和通则0862中测定方法的相关要求,采用直接稀释法处理磺丁基倍他环糊精钠注射剂辅料,使用岛津ICPMS-2040测定了该辅料中多种杂质元素含量。该方法操作简单,定量准确,可以满足ICH Q3D 对注射液辅料中杂质元素限量值的测定要求。
<样品处理和参数设置>
实验所用器皿分别为塑料或玻璃材质,使用硝酸溶液(1+1)浸泡24小时后,用去离子水冲洗,干燥备用;实验所用 HNO,为优级纯试剂,实验用水为超纯去离子水。准确称取30mg试样,加入Au溶液作为稳定剂(最终溶液中Au浓度为1mg/L),用1%硝酸定容至10g,摇匀,待测。同法制备样品空白溶液和样品加标溶液。

<分析结果>
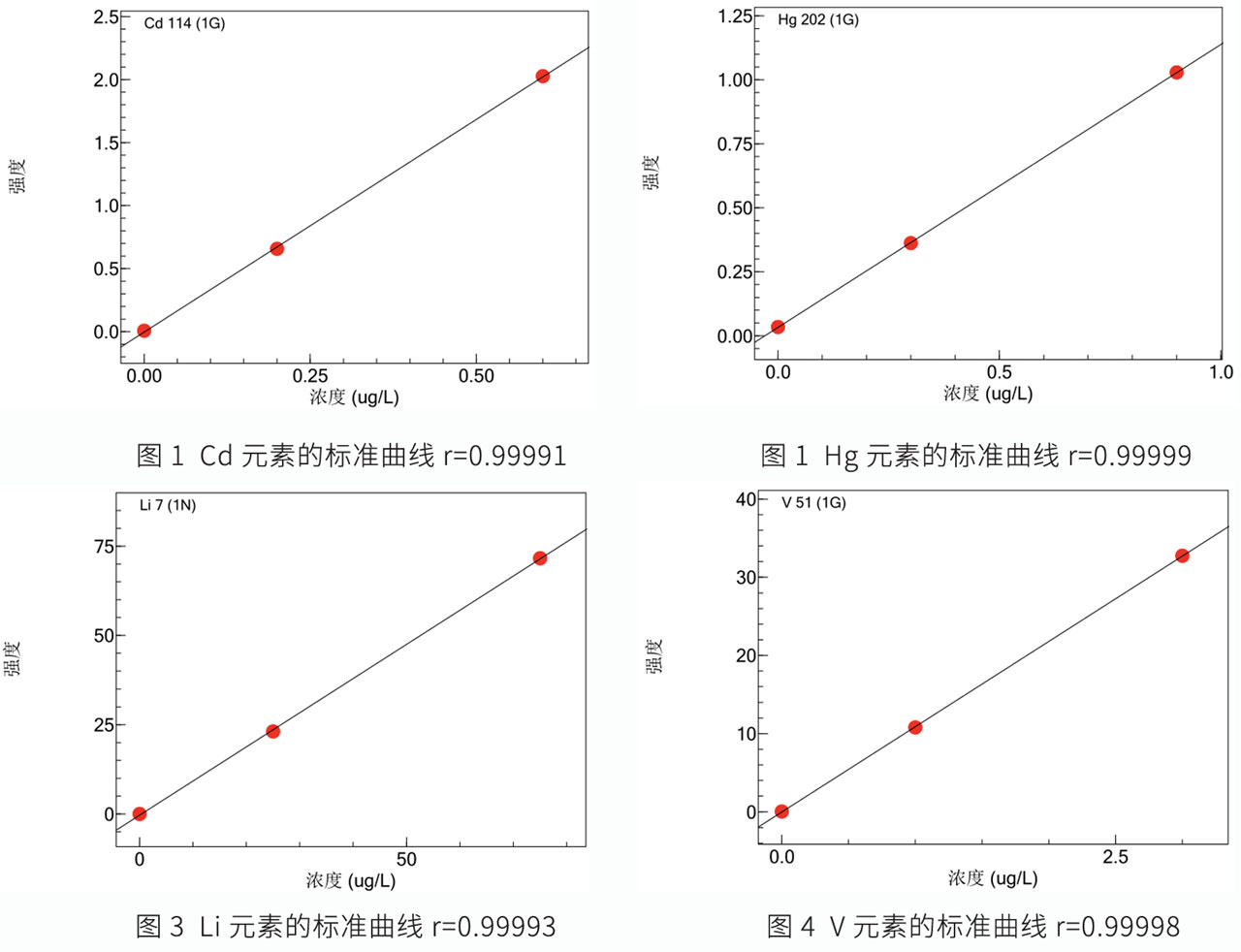
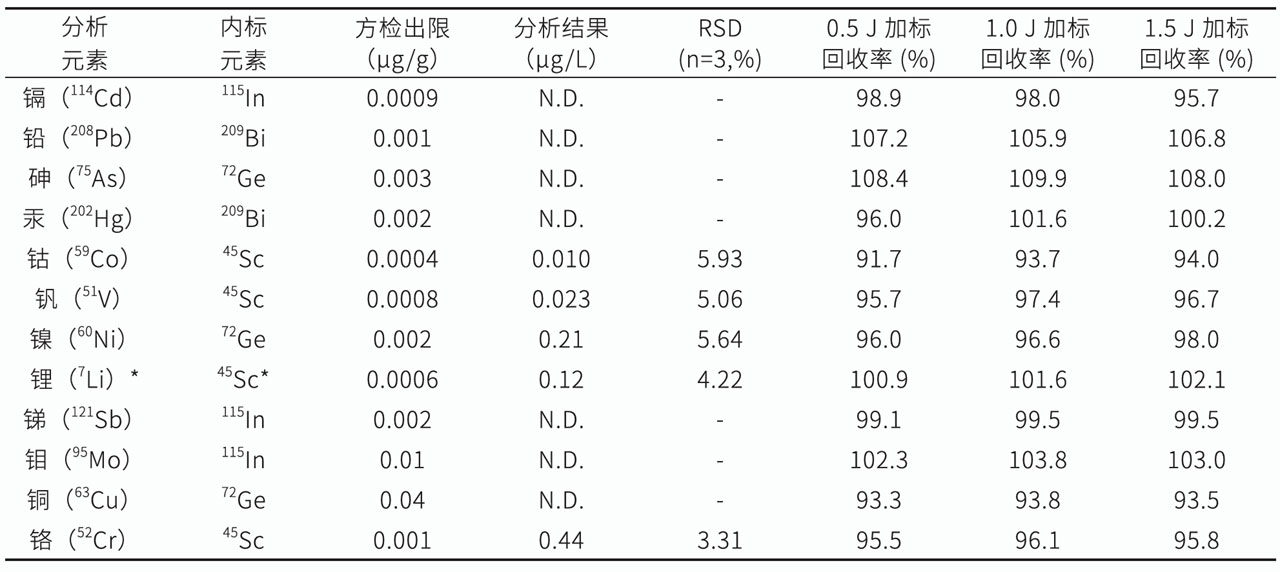
数据表明,0.5倍、1倍和1.5倍的限量值的加标回收率在91.7-109.9%之间,完全满足药典(ChP/USP)对样品加标回收率需要70%-150%的要求。
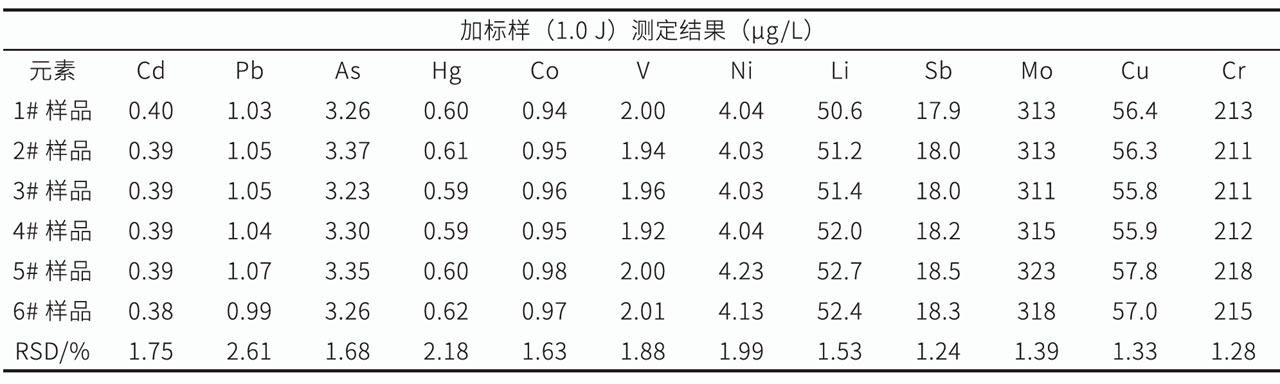
结果表明,6份样品1倍限量值加标样测定结果的相对标准偏差小于3%,即该方法的精密度(%RSD)值完全符合药典(ChP/USP)规定的要求,即每种目标元素的RSD值小于20%。
● 典型案例2-【ICP-MS测定葡甲胺中的铅和镍的含量】
2025年版《中国药典》修订了葡甲胺标准,新增了镍盐检查项,“注”提示为满足制剂安全性和有效性要求,必要时,可对本品中的元素杂质铅进行控制。
葡甲胺为1-脱氧1-9(甲氨基)-D-山梨醇,其为白色结晶性粉末,易溶于水,广泛作为药物的pH调节剂和增溶剂。由于葡甲胺具有钠类似的渗透性和离子半径,且不会透过细胞膜,因此它正被越来越多地作为钠的替代物使用。葡甲胺是由葡萄糖与一甲胺缩合后再进行催化加氢而得,其生产过程中需要使用雷氏镍,可能导致镍铅等重金属的残留。采用岛津ICPMS建立了对相关元素杂质进行同时测定的方法,可供参考。


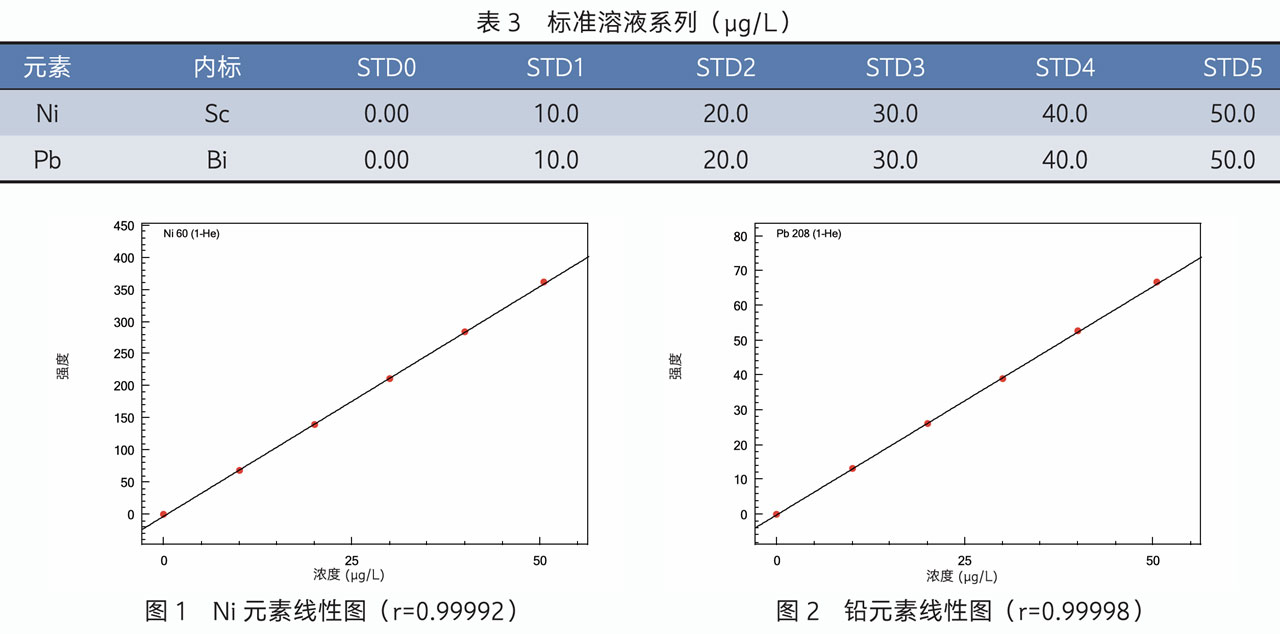
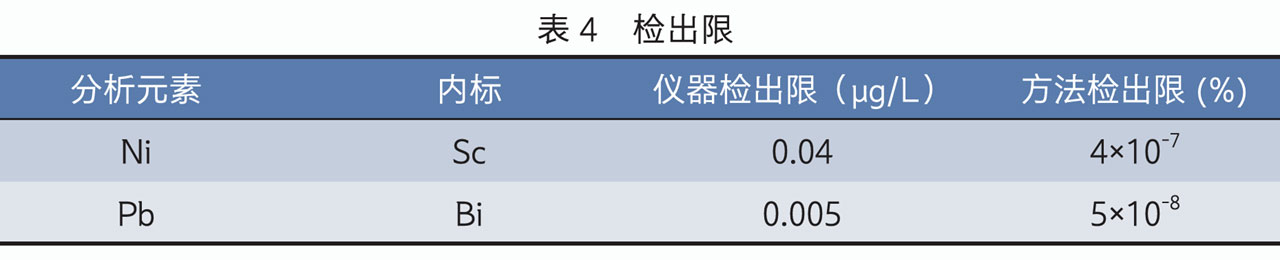

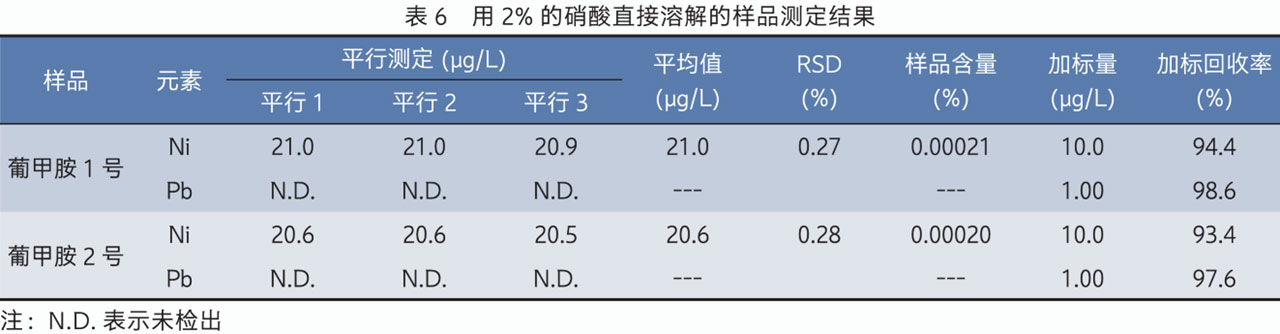
采用ICPMS-2050LF电感耦合等离子体质谱仪,微波消解前处理样品测定了葡甲胺中镍和铅的含量,该方法准确度高,检出限低,稳定性好,并用2%硝酸直接溶解后辅证测定了分析结果,两种前处方法测定结果基本一致。
参考文献:
【1】蔡立荣,陈蕾,等.《中华人民共和国药典》药用辅料相关标准中元素杂质与ICH Q3D协调策略分析[J].医药导报,2025,44(2):223-227x



