解决方案-0461 X射线荧光光谱法修订
X射线荧光光谱法(XRF)作为元素分析的无损筛查技术,在药品元素杂质控制(ICH Q3D)、药用包材重金属迁移、矿物药鉴定中具有重要作用。2025年版中国药典全面升级通则0461 X射线荧光光谱法,推动方法从定性半定量向精准定量转型,强化与ICH Q3D、USP<735>的协调性,明确方法验证要求。
1、修订说明
2020年版《中国药典》首次收载了 X射线荧光光谱法。为使该标准进一步与国际标准接轨,此次借鉴国内外相关标准和研究成果,并根据我国实际情况进行修订。修订的主要内容包括对前言、供试品的制备、定量测定法相关内容的补充完善,以及增订方法学验证与确认中准确度、重复性、中间精密度、专属性、定量限、线性、范围、耐用性、确认相关的内容。
注:内容引自国家药典委员会网站
| 修订方向 | 2020年版中国药典 | 2025年版中国药典 | 修订说明 |
|---|---|---|---|
| 方法验证 | 无系统要求 | 增准确度/精密度/LOQ等7项验证指标 | 满足ICH Q2、FDA GMP要求 |
| 仪器分类 | 未区分仪器类型 | 明确WD/ED-XRF适用场景和技术指标 | 指导仪器科学选型 |
| 定量方法 | 基础定量方法 | 增加FP法、XFP等数学校正法 | 提升非标样准确性 |
| 样品制备 | 简单描述 | 细化粒度、均质性、压力控制参数 | 减少制样误差 |
通则0461在两版药典中的主要差异对比
2、核心修订要点
(1)方法学验证体系化
首次建立了完整的XRF方法验证参数体系,填补了既往版本的规范空白:
准确度分级要求:化学原料药回收率需达98.0%-102.0%;中药复方制剂放宽至90.0%-110.0%;杂质分析则为70.0%-150.0%。
精密度层级控制:重复性要求原料药RSD≤1.0%,药物制剂≤2.0%;中间精密度要求制剂RSD≤3.0%。
定量能力系统评估:定量限(LOQ)需通过空白标准偏差的10倍估算,并在50%LOQ浓度水平验证准确性
(2)仪器分类与适用场景
波长色散型(WD-XRF):功率大、精度高,适用于原料、制剂的精确检测和质量控制。
能量色散型(ED-XRF):无需复杂前处理、无损分析,可直接用于片剂包衣检测、生产在线监控。
(3)样品制备标准化
固体样品粒度控制:化学药品一般建议过200目筛;中药材及复方制剂一般全部过100目筛。
3、岛津解决方案
岛津EDX系列产品完全符合2025年版中国药典通则0461对仪器硬件的一般要求。

适用的样品类型广泛,固体片剂、粉末和液体均可

实验操作过程简单

ALTRACE能量色散型X射线荧光光谱仪(新品) EDX-7200/8100系列(注:EDX为岛津ED-XRF产品)
PCEDX Pro提供多种计算方法,包括标准曲线法、FP法(基本参数法)、薄膜FP法、背景FP法等,能完美应对0461通则新增的数学校正法相关内容,帮助客户快速准确地进行数据分析。此外,PCEDX Pro CS/DB版完全满足制药行业对于FDA 21CFR Part11的合规需求,包括安全功能、审计追踪、用户管理、验证功能等,且通过岛津LabSolutions CS平台让数据管理更加高效。
典型应用场景:
• 原料药或制剂中元素含量测定和元素杂质的快筛(可搭配“药物元素杂质分析方法包”应对ICH Q3D需求)
• 生产中控现场的反应中间产物相关元素(如卤素、金属)的含量控制
• 中间体或原料药生产所用贵金属催化剂的残留分析及回收
• 含矿物药的中成药中如Hg/As/Cu等元素的含量快速测定
• 生产过程或成品中微小异物分析(可与显微红外技术搭配进行综合分析)
4、典型应用案例
利用EDX对口服制剂中金属元素快筛分析

根据中国药典0461/USP<735>进行验证
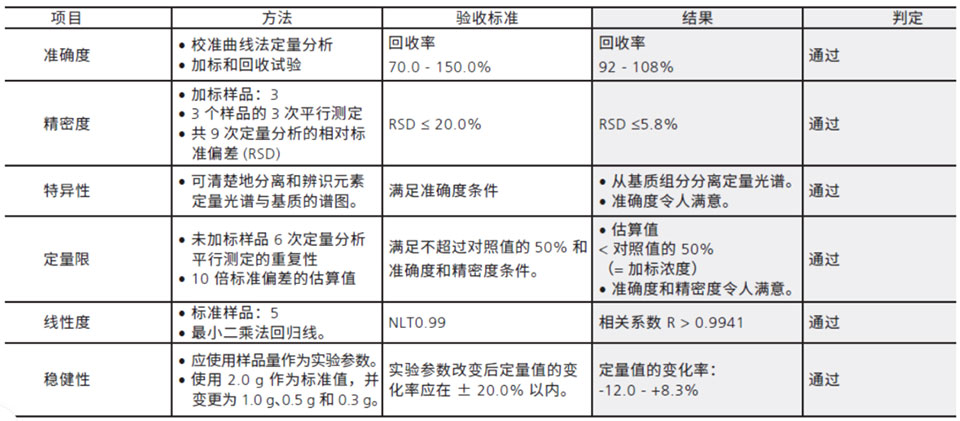
结果展示:
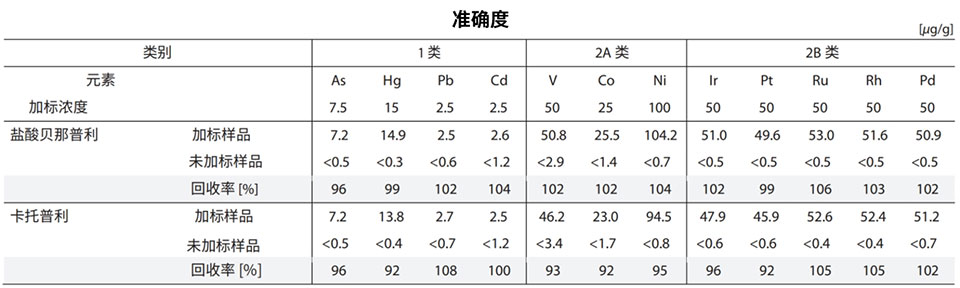
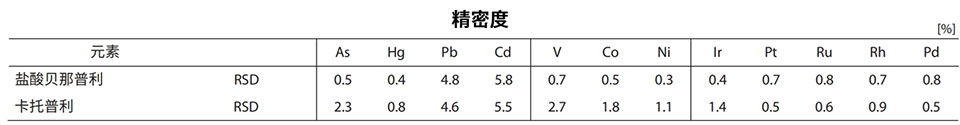
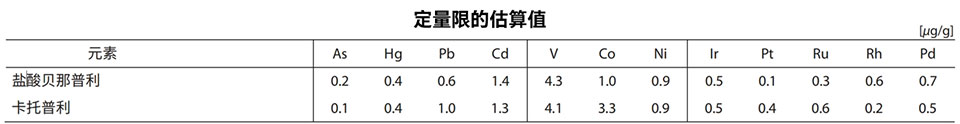
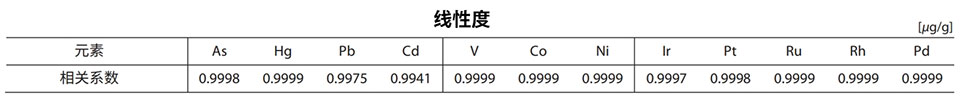
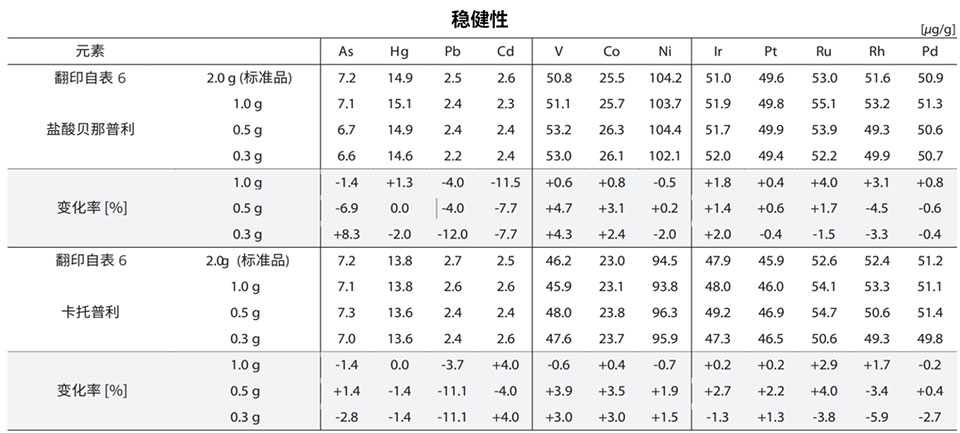
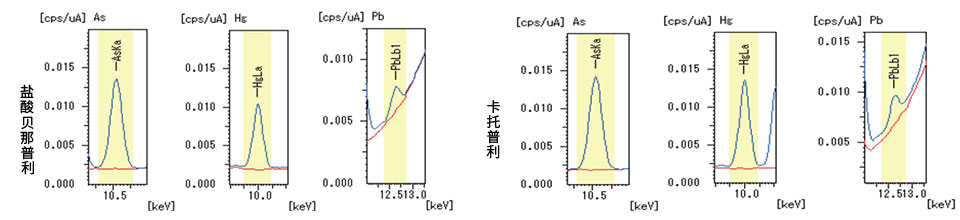
特异性结果验证



